
Calcula la presión de vapor de cada componente y la presión de vapor total sobre la disolución. Considera una disolución que contiene 1 00 mol de heptano y 4 00 moles de octano. A 40 c la presión de vapor del heptano puro es de 92 0 torr y la presión de vapor del octano puro es de 31 0 torr.

Esta es la fórmula general que necesitarás para resolver la mayoría de los problemas de presión de. La fórmula utilizada para calcular la presión de vapor dando un cambio en la presión de vapor sobre el tiempo se conoce como la ecuación de clausius clapeyron nombrada así por los físicos rudolf clausius y benoît paul émile clapeyron. Escribe la ecuación de clausius clapeyron.

Qué presión ejerce la caja sobre el suelo. Facebook twitter 32 google ejercicios resueltos de presión y fuerzas física y química 4º eso pruebas de acceso ejercicio resuelto ver solución una caja de 30 kg está apoyada sobre una de sus caras que tiene 40 cm de ancho y 50 cm de largo. La ecuación a utilizar es.

Qué deformación unitaria se obtiene al aplicar un esfuerzo de tensión de 420 mpa. El módulo de elasticidad de una varilla es de 4 x 10 11 pa. Ejercicios resueltos ejercicio 1.

τ 35 mpa. Sabiendo que 1 mega pascal mpa es 10 6 pascal el esfuerzo de tensión queda. Los ejercicios de densidad y presion estan bien pero los de principio de pascal y prensa hidraulica estan mal debido a que el area se debe realizar con el.
Y en cada envolo hay q calcular el area con la formula que bien te la da alli mismo. Otro de los ejemplos que podemos encontrar sin duda. Prensa hidráulica ejercicios resueltos.

Quieres proponer un ejercicio para que te los resolvamos.
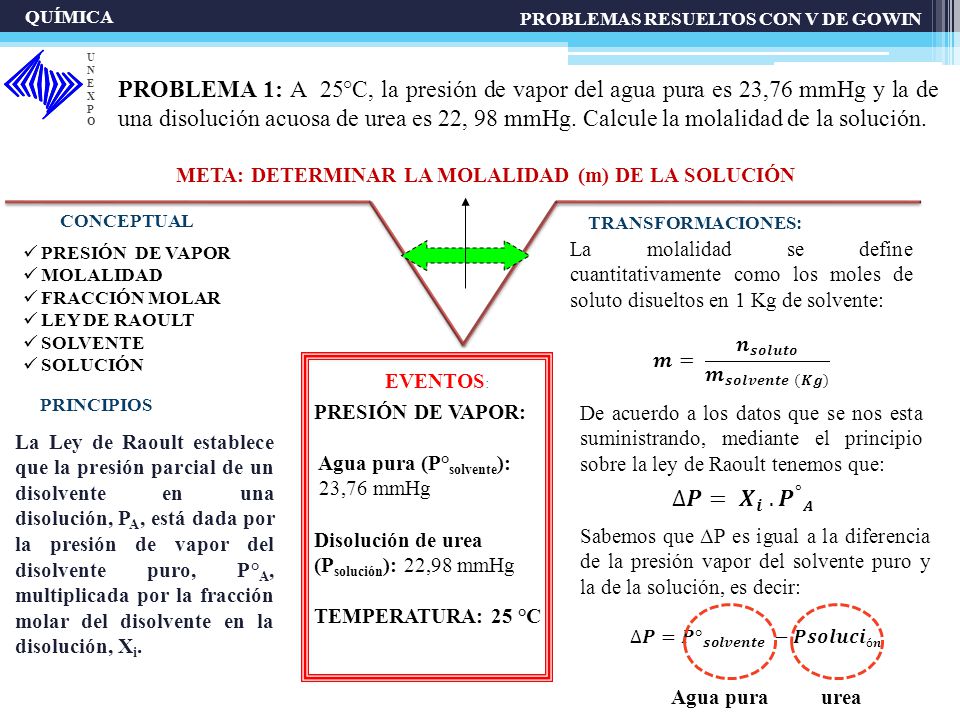
Presion de vapor formula ejercicios resueltos. La presión de vapor es aquella que experimenta la superficie de un líquido o sólido como producto de un equilibrio termodinámico de sus partículas en un sistema cerrado. Se entiende por sistema cerrado un recipiente contenedor o botella que no están expuestos al aire y a la presión atmosférica. Ejercicios resueltos 01 ver solución. Calcula la presión osmótica de una disolución que contiene 12 g de sacarosa c 12 h 22 o 11 en 500 ml de disolución a 20 ºc.
Msi 1 bachillerato. Ejercicios resueltos 02 ver solución. La glucosa es y su masa molecular es 180 g mol. El alcohol etílico es y su masa molecular es 46 g mol.
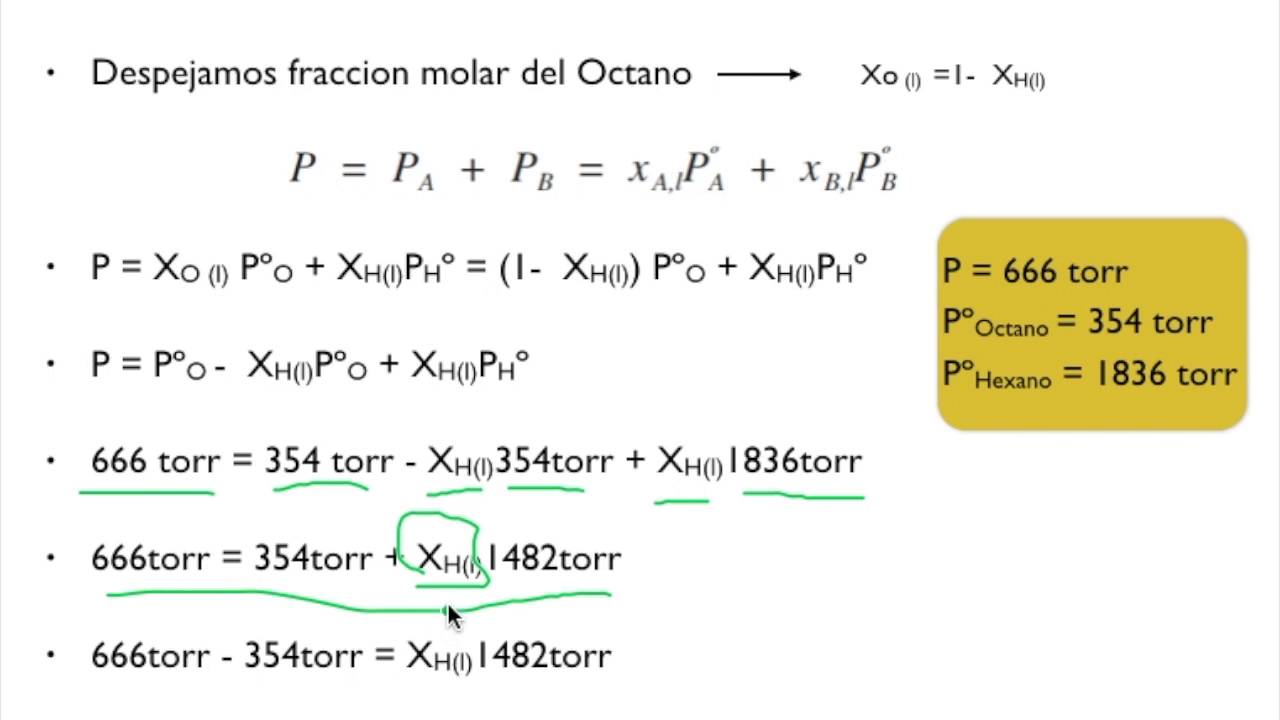
Con estos datos vamos a calcular los moles de cada sustancia y tendremos la fracción molar del alcohol en la mezcla. La fracción molar del alcohol es. Ahora calculamos la presión de vapor a partir de la expresión de la ley de raoult. Lo que hacemos por nosotros mismos muere con nosotros.
Lo que hacemos por los demás y por el mundo permanece y es inmortal albert payne. Más de 5000 ejercicios resueltos de física y química para educación secundaria y bachillerato. Buscar ejercicios saber más. Miles de ejercicios resueltos de educación secundaria bachillerato y otros niveles.
Resolvemos tus dudas tienes alguna duda.
Resolvemos tus dudas tienes alguna duda. Miles de ejercicios resueltos de educación secundaria bachillerato y otros niveles. Buscar ejercicios saber más.

Más de 5000 ejercicios resueltos de física y química para educación secundaria y bachillerato. Lo que hacemos por los demás y por el mundo permanece y es inmortal albert payne. Lo que hacemos por nosotros mismos muere con nosotros.

Ahora calculamos la presión de vapor a partir de la expresión de la ley de raoult. La fracción molar del alcohol es. Con estos datos vamos a calcular los moles de cada sustancia y tendremos la fracción molar del alcohol en la mezcla.

El alcohol etílico es y su masa molecular es 46 g mol. La glucosa es y su masa molecular es 180 g mol. Ejercicios resueltos 02 ver solución.

Msi 1 bachillerato. Calcula la presión osmótica de una disolución que contiene 12 g de sacarosa c 12 h 22 o 11 en 500 ml de disolución a 20 ºc. Ejercicios resueltos 01 ver solución.

Se entiende por sistema cerrado un recipiente contenedor o botella que no están expuestos al aire y a la presión atmosférica. La presión de vapor es aquella que experimenta la superficie de un líquido o sólido como producto de un equilibrio termodinámico de sus partículas en un sistema cerrado.







